Khối lượng mol là gì? Ví dụ minh họa. – Trường THPT Diễn Châu 2 – Nghệ An
Câu vấn đáp :
Khối lượng mol ( kí hiệu M ) của một chất là khối lượng tính bằng gam của N nguyên tử hay phân tử chất đó. Như vậy, khối lượng mol của nguyên tử hoặc phân tử của một chất có cùng số hiệu với nguyên tử khối hoặc phân tử khối của chất đó .
– Ví dụ:
Khối lượng mol nguyên tử Na : MNa = 23 g / mol .
Khối lượng mol của natri clorua ( NaCl ) : MNaCl = 58,5 g / mol .
Hãy cùng Top Solutions tìm hiểu và khám phá thêm về nồng độ mol và khối lượng mol nhé !
Khái niệm : mol là lượng chất chứa 6,02. 1023 nguyên tử hay phân tử chất đó .
– Dãy số 6.02.1023 được gọi là dãy số Avôgađrô và được kí hiệu là N .
– Nếu biết số mol ta tính được số phân tử hoặc nguyên tử .
Ví dụ : Tính số nguyên tử Cu có trong 2 mol Cu
Cứ 1 mol Cu thì có 6,02. 1023 Cu. nguyên tử
=> 2 mol Cu có : 2,6,02. 1023 Cu. nguyên tử
Chú ý : Phân biệt nghĩa của hai cách viết sau :
+ 1 mol H => chỉ có 1 mol nguyên tử Hiđro .
+ 1 mol H2 => chỉ có 1 mol phân tử hiđro .
Khối lượng mol ( kí hiệu M ) của một chất là khối lượng tính bằng gam của N nguyên tử hay phân tử chất đó .
Đơn vị : g / mol
Khối lượng mol có cùng số với khối lượng nguyên tử hoặc khối lượng phân tử của chất .
Lưu ý, khối lượng mol của phân tử không giống như khối lượng mol của nguyên tử .
Ví dụ :
Khối lượng mol của nước ( H2O ) là 18 g / mol .
Khối lượng mol của một nguyên tử hydro ( H ) là 1 g / mol .
Khối lượng mol của hydro ( H2 ) là 2 g / mol .
• Có nghĩa là :
– Khối lượng của N phân tử H2O hay 6,1023 phân tử H2O là 18 gam .Khối lượng N nguyên tử hiđro ( H ) là 1 g .
– Khối lượng phân tử hiđro N ( H2 ) là 2 g .
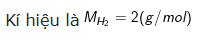
m = m / n
Bên trong :
+ M là khối lượng mol của chất ( tính theo khối lượng nguyên tử hoặc khối lượng phân tử của chất đó ), tính bằng g / mol .
+ m là khối lượng của chất, đơn vị chức năng ( g ) .
+ n là số mol của chất, tính bằng ( mol ) .
Bài tập 1 : Tìm công thức hóa học của hợp chất có thành phần theo khối lượng là 36,8 % Fe, 21,0 % S, 42,3 % O. Biết khối lượng mol của hợp chất là 152 g / mol
Câu vấn đáp :
Vậy trong 1 phân tử hợp chất có 1 nguyên tử Fe, 4 nguyên tử O, 1 nguyên tử S.
Xem thêm: Chiều cao xe tải bao nhiêu là phù hợp? – Dịch Vụ Chuyển Nhà Trọn Gói Kiến Vàng Giá Rẻ Hà Nội
→ Công thức là FeSO4
Bài 2 : Một hợp chất có công thức hóa học là K2CO3. Tính khối lượng mol của chất đã cho .
Câu vấn đáp :
Khối lượng mol của K2CO3 là :
MK2CO3 = 39,2 + 12 + 16,3 = 138 ( g )
Bài tập 3 : Có phương trình hóa học sau : CaCO3 + 2HC l → CaCl2 + CO2 + H2O. Tìm khối lượng canxi clorua thu được khi cho 10 g canxi cacbonat phản ứng với axit clohiđric dư
Câu vấn đáp :
Số mol canxicacbonat tham gia phản ứng là :
nCaCO3 = 10/100 = 0,1 mol .
Phương trình hóa học của phản ứng :
CaCO3 + 2HC l → CaCl2 + CO2 + H2O
Theo phương trình hóa học ta có :
nCaCl2 = nCaCO3 = 0,1 mol .
Khối lượng canxi clorua tham gia phản ứng :
mCaCl2 = 0,1. ( 40 + 71 ) = 11,1 gam .
Bài tập 4 : Cho khối lượng của những chất sau :
a ) 1 mol Na. nguyên tử
b ) 0,5 phân tử NaCl
c ) 0,05 mol phân tử glucozơ C6H12O6
Câu vấn đáp :
a ) Khối lượng 1 mol nguyên tử Na : 23 gam
b ) Khối lượng của 0,5 phân tử NaCl : 0,5. ( 23 + 35,5 ) = 29,25 gam
c ) Khối lượng của 0,05 mol phân tử glucozơ C6H12O6 : 0,05. ( 12,6 + 12 + 16,6 ) = 9 gam
Bài 5 : Tính khối lượng những chất sau :
a ) 0,3 mol nguyên tử Na ; 0,3 mol O2. phân tử
b ) 1,2 mol phân tử HNO3 ; 0,5 mol Cu. phân tử
c ) 0,125 mol mỗi chất sau : KNO3, KMnO4, KClO3
Câu vấn đáp :
Áp dụng công thức tính khối lượng : m = nM ( gam )
a ) Khối lượng của 0,3 mol nguyên tử Na bằng : mNa = nNa. MNa = 0,3. 23 = 6,9 gam
Khối lượng của 0,3 mol phân tử O2 bằng : mO2 = nO2. MO2 = 0,3. 32 = 9,6 gam
b ) Khối lượng của 1,2 mol HNO3 bằng : mHNO3 = nHNO3. MHNO3 = 1,2. 63 = 75,6 gam
Khối lượng của 0,5 mol Cu bằng : mCu = nCu. MCu = 0,5. 64 = 32 gam
c ) Khối lượng của 0,125 mol KNO3 bằng : mKNO3 = nKNO3. MKNO3 = 0,125. 101 = 12,625 gam
Khối lượng của 0,125 mol KMnO4 bằng :mKMnO4 = nKMnO4.MKMnO4 = 0,125,158 = 19,75 gam
Bạn thấy bài viết Khối lượng mol là gì? Ví dụ minh họa. có khắc phục đươc vấn đề bạn tìm hiểu ko?, nếu ko hãy comment góp ý thêm về Khối lượng mol là gì? Ví dụ minh họa. bên dưới để Trường THPT Diễn Châu 2 có thể thay đổi & cải thiện nội dung tốt hơn cho các bạn nhé! Cám ơn bạn đã ghé thăm Website: dienchau2.edu.vn của Trường THPT Diễn Châu 2
Nhớ để nguồn bài viết này: Khối lượng mol là gì? Ví dụ minh họa. của website dienchau2.edu.vn
Chuyên mục : Là gì ?
Source: https://suachuatulanh.edu.vn
Category : Vận Chuyển